Тело человека и животных, предметы, материалы и даже целая Земля. Что общего между этими понятиями? А то, что все они состоят из химических элементов. Более того, вся Вселенная – это набор простых и сложных химических элементов. Хотите узнать о них больше? Читайте наш материал.
Что такое химические элементы?
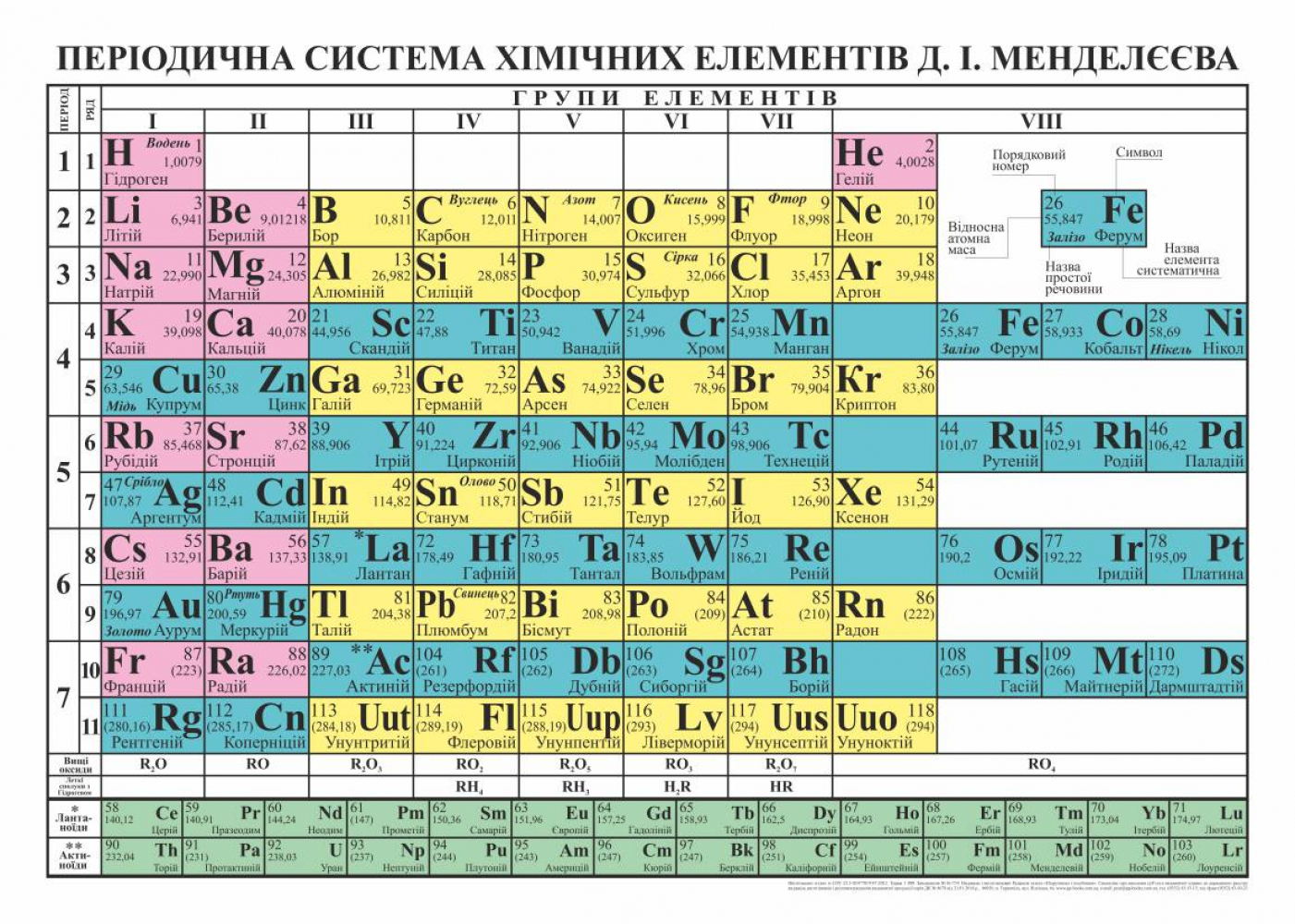
Химические элементы – это разновидности атомов, имеющих одинаковое количество протонов в своем ядре. Элементы классифицируются по их атомным номерам, которые соответствуют количеству протонов в ядре. Например, атомы с одним протоном в ядре относятся к водороду (H), атомы с шестью протонами – к углероду (C), атомы с восемью протонами – к кислороду (O) и т.д.
Протоны – это один из трех основных типов элементарных частиц, из которых состоит атомное ядро. Они обладают положительным электрическим зарядом. Протоны совместно с нейтронами (не имеющими заряда) образуют ядро атома. Электроны, вращающиеся вокруг ядра, имеют отрицательный заряд и обеспечивают атому электрическую стойкость из-за образования электронной оболочки атома.
На сегодня ученые доказали о существовании 118 химических элементов. 92 из них встречаются в природе, а остальные 26 были выведены искусственным путем. Каждый элемент имеет свои уникальные свойства, определяемые атомным строением. Химические элементы могут сочетаться между собой, образуя различные соединения и вещества, которые играют немаловажную роль в жизни человека и функционировании Вселенной в целом.
Как обозначаются химические элементы?
Химические элементы обозначаются с помощью символов, состоящих из одной или двух букв латинского алфавита. Эти символы являются стандартными и используются в химии для идентификации элементов в таблице, называемой «Периодической системой». Каждый химический элемент имеет уникальный символ, обычно отображающий первую букву (или первые две буквы) названия элемента.
К примеру:
- H (Hydrogenium) – водород.
- O(Oxygenium) – кислород.
- C (Carboneum) – углерод.
- Fe (Ferrum) – железо.
- Na (Natrium) – натрий.
Какие есть виды химических элементов?
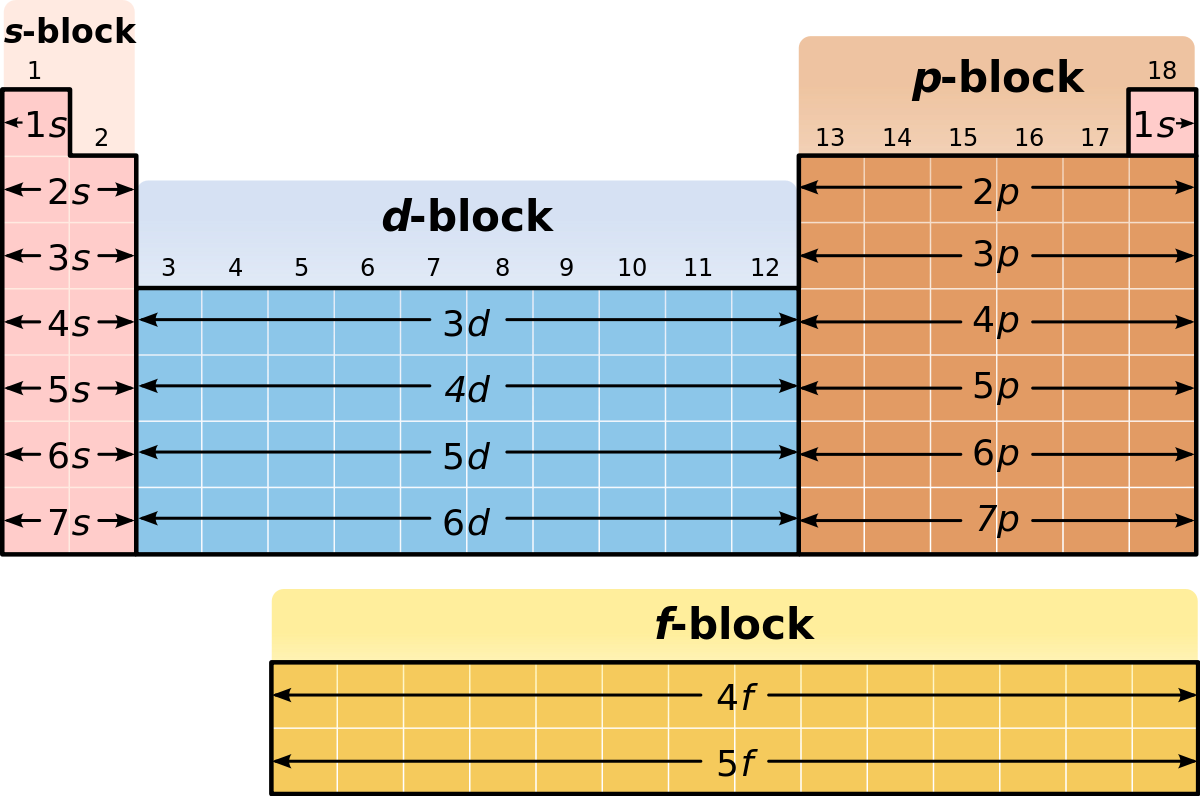
Химические элементы разделяют по разным характеристикам: физическим свойствам, химическим свойствам, происхождению и т.д. Однако основной и общепринятый способ разделения химических элементов – по их атомным номерам или по их позиции в периодической системе. Ниже расскажем о каждой группе элементов в таблице.
Другим способом разделения является классификация элементов на металлы, неметаллы и полуметаллы в зависимости от химических свойств.
|
Характеристика |
Примеры |
|
|
Металлы |
Металлы – это элементы, обладающие хорошо выраженными металлическими свойствами. Они имеют металлический блеск, хорошо проводят тепло и электрический ток, а также обладают высокой пластичностью. |
железо (Fe), медь (Cu), алюминий (Al), золото (Au), серебро (Ag), натрий (Na), калий (K) |
|
Неметаллы |
Неметаллы – это элементы, не обладающие характеристиками металлов. Обычно они не имеют металлического блеска, являются плохими проводниками тепла и электрического тока и непригодны к ковке. |
кислород (O), углерод (C), азот (N), фосфор (P), сера (S), хлор (Cl), бром (Br), йод (I) |
|
Полуметаллы |
Полуметаллы или металлоиды – это элементы, обладающие свойствами как металлов, так и неметаллов. Они могут являться полупроводниками, то есть их свойства электропроводности изменяются в зависимости от условий. |
кремний (Si), германий (Ge), арсен (As), селен (Se), антимоний (Sb), теллур (Te) |
Читайте также: НМТ 2024: список предметов и даты экзаменов